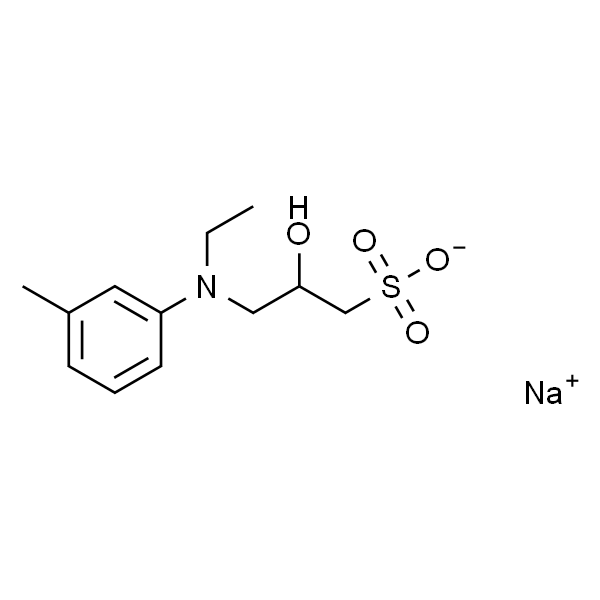
N-乙基-N-(2-羟基-3-磺丙基)-3-甲基苯胺钠盐
用于酶法光度法测定过氧化氢的一种高性能、高水溶性关键试剂
- 英文名称: TOOS
- CAS号: 82692-93-1
- 分子式: C12H19NNaO4S
- 分子量: 296.3378
- EINECS号: 617-377-8
- MDL No.: MFCD00040641
- 纯度/规格: ≥99%
- 包装: 按需分装
- 产品参数
- 英文名称: TOOS
- CAS号: 82692-93-1
- 分子式: C12H19NNaO4S
- 分子量: 296.3378
- EINECS号: 617-377-8
- MDL No.: MFCD00040641
- 纯度/规格: ≥99%
- 包装: 按需分装


 复制产品链接
复制产品链接
 长按图片保存/分享
长按图片保存/分享
询盘

客服电话:400-9090-710
内销电话:13319523173 鲁经理
外贸电话:0731-85525705 13319518603 梁经理
外贸邮箱:ivy@hnhbsj.com








 客服1
客服1 客服2
客服2 外贸邮箱
外贸邮箱